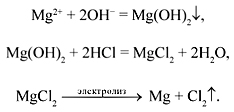Урок по теме «Бериллий, магний и щелочноземельные металлы»
Таким образом, класс еще раз повторит и закрепит алгоритм расстановки коэффициентов в уравнениях окислительно-восстановительных реакций методом электронного баланса, поскольку ОВР являются одним из основных элементов содержания ЕГЭ.
3. Опыт «Взаимодействие с кислотами».
Учитель. Все металлы этой подгруппы взаимодействуют с растворами сильных кислот.
Учащиеся записывают уравнения химических реакций:
Mg + H2SO4 = MgSO4 + H2,
Ca + 2HCl = CaCl2 + H2.
Учитель. А теперь давайте вспомним, почему щелочно-земельные металлы так называются.
Ученик. Словом «земля» алхимики обозначали плохо растворимые соединения. Поскольку при смачивании водой оксидов кальция, стронция и бария образовывалась щелочная среда, то эти оксиды стали называть щелочными землями, а металлы – щелочно-земельными.
Учитель. В чем особенность бериллия?
Ученик. Бериллий является элементом, оксид и гидроксид которого проявляют амфотерный характер: они образуют соли при взаимодействии как с кислотами, так и со щелочами.
Учитель. Докажите это соответствующими уравнениями реакций.
Ученик (выходит к доске и записывает уравнения). Взаимодействие оксида бериллия с хлороводородной кислотой:
BeO + 2HCl = BeCl2 + H2O,
взаимодействие оксида бериллия с гидроксидом натрия:
BeO + 2NaOH = Na2BeO2 + H2O.
Учитель. А теперь мы проведем такой эксперимент. Перед вами находятся образцы cолей трех металлов. Все они на вид одинаковые. А как же определить, где соль кальция, где бария, а где стронция? Для этого обратимся к справочному материалу.
На данном этапе необходимо провести качественное обнаружение ионов щелочно-земельных металлов: облить тампоны, лежащие в чашечках, этиловым спиртом и поджечь. Обратить внимание на цвет пламени спирта.
Станция «Потребительская»
Далее учитель обращает внимание на опорный конспект, который лежит на столах учеников, активно обсуждает его с классом. Необходимый для запоминания материал учащиеся помечают у себя в тетрадях.
Опорный конспект
|
Получение металлов II группы, главной подгруппы 1. Кальций и стронций получают электролизом расплавов их хлоридов:
2. Для получения бария используют алюмотермию:
3. Бериллий получают восстановлением магнием из фторида:
4. Магний получают в промышленности из морской воды. Ионы магния, содержащиеся в морской воде, осаждают в виде гидроксида, который затем переводят в хлорид, электролизом расплава хлорида магния получают металл:
|
Закрепление изученного материала
Учитель. Ну вот и подошло к концу наше путешествие в город «Щелочноземельск». Но не расстраивайтесь, ведь впереди нас с вами ждет увлекательнейшая экскурсия по другим городам «Металлии», таким, как «Железногорск» и «Алюминевск». Но прежде чем уехать в наш городок Рассказово, необходимо ответить на вопросы от жителей «Щелочноземельска».
Информация о ообразовании:
Особенности логопедической работы по коррекции нарушений письменной речи в
специальной школе VIII вида
При устранении нарушений письменной речи у умственно отсталых школьников необходимо учитывать особенности высшей нервной деятельности, психопатологические особенности детей. В связи с этим коррекция нарушений чтения и письма во вспомогательной школе должна быть тесно связана с развитием познаватель ...
Особенности управления ВУЗом
Термин «руководство образовательным учреждением» обозначается как механизм для организации и обеспечения оптимальных условий функционирования образования на всех уровнях, «мозг» системы. Особенностью управления современной системой образования является прежде всего обеспечение руководящими кадрами ...
Понятие «личностно-ориентированное обучение» в психолого-педагогической
литературе
Понятие «личностно-ориентированное обучение», вошедшее в 90-е годы в педагогический арсенал без своей четкой дефиниции, по-нашему мнению, может быть определено при рассмотрении таких категорий, как: индивид, индивидуальность (индивидуальный подход), личность. При этом в конкретных исторических усло ...
Категории
- Главная
- Нетрадиционные формы организации обучения
- Экономическое мышление школьников
- Восприятие текста
- Эстетическое воспитание школьников
- Работа социального педагога
- Новые средства и методы образования
- Подробно о педагогике